Interview de Gwenola Le Dréan – 2eme partie

Bonjour,
Nous continuons aujourd’hui l’interview de Gwenola Le Dréan, physiologiste et spécialiste de l’axe intestin-cerveau est chercheure à INRAE (Institut National de Recherche pour l’Agriculture, l’Alimentation et l’Environnement) au laboratoire « Physiopathologie des Adaptations Nutritionnelles » (UMR 1280) qu’elle co-dirige, à Nantes.
Quels sont aussi les effets d’une nutrition maternelle déséquilibrée en période prénatale ?
De nombreuse études ont documenté les effets d’une nutrition maternelle déséquilibrée sur le développement du cerveau fœtal et les conséquences comportementales plus tard dans la vie comme par exemple la sensibilité et la réponse au stress chez l’homme. C’est aussi le cas des processus de mémorisation chez la souris, en lien avec une altération des progéniteurs neuronaux, les cellules souches à l’origines des neurones.
Ainsi les aliments ultra-transformés, les sucres ajoutés et les graisses saturées, l’appauvrissement en vitamines et en micronutriments essentiels tels que le zinc et le sélénium, créent un stress oxydatif cellulaire à l’origine d’une inflammation chronique qui va affecter la barrière hématoencéphalique et le cerveau. L’exposition à un régime hypercalorique riche en gras et en sucre dans un contexte d’obésité maternelle est connue pour être associée à des conséquences négatives sur la santé mentale des enfants, notamment les troubles de déficit d’attention et hyperactivité (TDAH). Un contexte hyperglycémique in utero, notamment s’il apparait tôt dans la grossesse durant le 1er trimestre, est également associé au TDAH chez l’enfant. Néanmoins, dans ces situations d’obésité maternelle ou de diabète gestationnel, il est difficile de dissocier les effets de la nutrition maternelle en elle-même des troubles métaboliques dont est atteinte la maman, sur la santé future du bébé. Les modèles animaux restent essentiels pour parvenir à le faire.

© David Faure
Toujours pendant cette période prénatale, pouvez-vous nous en dire encore plus sur l’activation du système immunitaire par le microbiote et les liens avec l’alimentation ?
Au sens clinique, la période périnatale est définie par l’intervalle compris entre la 28ème semaine de grossesse et la première semaine de vie. Dans la littérature, la périnatalité fait parfois référence aux 1000 premiers jours de vie, de la conception jusqu’au sevrage de l’enfant et la diversification alimentaire. Rappelons que le lait maternel est considéré par les pédiatres comme l’étalon-or de la nutrition infantile. Sa composition est adaptée aux besoins de l’enfant au cours de son développement post-natal. Si la composition en protéines et en lactose du lait maternel est peu sujette aux variations de l’alimentation maternelle, la fraction lipidique, elle, dépend au moins pour 30 % des apports maternels. Or il est connu que certains lipides sont essentiels au neurodéveloppement et au fonctionnement du cerveau comme par exemple les acides gras à chaînes longues polyinsaturées omega-3. L’acide docosahexaénoïque (DHA) est l’acide gras omega-3 qui prédomine dans le cerveau humain. Son accumulation démarre durant le 3ème trimestre de gestation et se poursuit jusqu’aux deux ans de l’enfant. Durant cette période, le DHA est impliqué dans la mise en place de la neurotransmission sérotoninergique et dopaminergique. Des effets bénéfiques, bien que pas systématiques, d’une supplémentation post-natale en DHA sur la fonction cognitive ont été reportés, principalement chez les enfants nés prématurés chez qui l’accumulation en DHA dans le cerveau au cours de la grossesse écourtée a été insuffisante. Cependant à l’heure actuelle, la modulation de la composition du microbiote fécal de ces enfants recevant du DHA ne permet pas de faire un lien causal direct avec le neurodéveloppement.
En revanche, un mécanisme indirect impliquant une activation du système immunitaire par le microbiote et induisant une neuroinflammation qui, à des périodes critiques d’assemblage et du microbiote et de sa colonisation du tube digestif, pourrait jouer un rôle majeur et contribuer à des troubles neuro développementaux, comportementaux et cognitifs. Ainsi, si nous reprenons l’exemple du DHA, sa supplémentation augmente l’abondance en espèces anti-inflammatoires telles que Bifidobacterium, Lactobacillus ou encore Akkermansia muciniphila. Les métabolites produits par ces bactéries, des acides gras à chaînes courtes, vont moduler la réponse inflammatoire en réduisant par exemple la production d’interleukine-6, cytokine pro-inflammatoire. Les effets anti-inflammatoires très bien documentés du DHA pourraient ainsi être médiés au moins en partie par ses interactions avec le microbiote intestinal de l’hôte (5). D’autre part, il faut aussi intégrer que les bactéries présentes dans le lait maternel, comme les Lactobacillus, Staphylococcus, Enterococcus et Bifidobacterium sont transférées au petit par l’allaitement et peuvent contribuer à l’assemblage du microbiote de l’enfant. Ces bactéries sont considérées comme des composants bioactifs du lait maternel ayant des effets protecteurs sur le système immunitaire du nouveau-né.
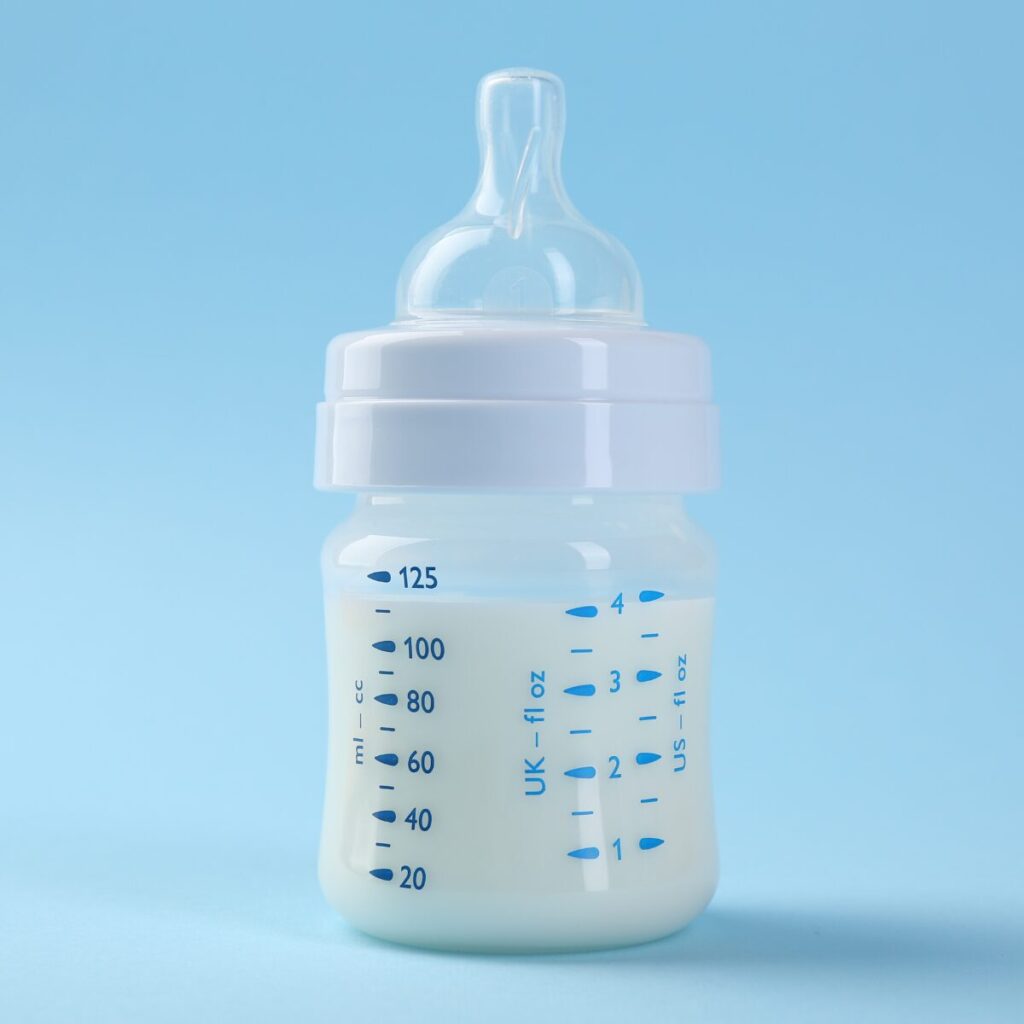
Les formulations infantiles du lait en poudre mises sur le marché pour remplacer ou suppléer l’allaitement proposent des compositions proches mais non identiques du lait maternel. Elles différent notamment par la teneur en protéines qui reste plus élevée dans les formules afin de maintenir un taux en acides aminés essentiels suffisant. D’autres éléments sont spécifiques du lait humain comme par exemple des oligosaccharides – en anglais HMO Human Milk Oligosaccharides – qui constituent des substrats de choix pour les Bifidobactéries majoritairement présentes chez l’enfant allaité. Certains de ces HMO ont été associés à un meilleur développement cognitif chez l’enfant notamment dans un contexte d’obésité maternelle, mais ces données restent à confirmer. Leur concentration dans le lait maternel varie avec l’alimentation de la mère. Un régime de type Méditerranéen avec peu de viande rouge, une consommation d’acides gras insaturés omega-3, et de fruits et légumes, leur sont plus favorables qu’un régime de type occidental gras et sucré (6). Les supplémentations des formules infantiles en HMO ou d’autres prébiotiques appelées aussi « fibres », sont des sucres non digestibles par notre intestin mais très appréciées des bactéries. Ils permettent de moduler la composition du microbiote des enfants non allaités vers celui des enfants allaités. La diversification alimentaire et l’introduction d’aliments solides augmentent la diversification des espèces composant le microbiome. Les capacités métaboliques de ce microbiote s’adaptent aux nutriments qui arrivent dans l’intestin.

Après ces explications passionnantes, comment souhaitez-vous conclure ?
En conclusion, il est important de souligner que les recherches qui étudient l’impact de la nutrition des 1000 premiers jours sur l’axe microbiote-intestin-cerveau sont actuellement en plein développement. La mise en évidence du dysfonctionnement de cet axe dans un nombre croissant de maladies en fait ainsi une cible thérapeutique majeure pour le futur. Les connaissances grandissantes sur l’origine développementale des maladies et de la santé, et notamment le rôle de la nutrition maternelle et de l’enfant sur sa santé future font de ces recherches un enjeu majeur de prévention des maladies.
Fin de la deuxième partie de cet interview. Pour accéder à la première partie, cliquez ici.


